第三篇 参比电极和电位测量
(1)参比电极
进行电化学测量通常需要使用参比电极。由于标准氢电极使用时需要使用氢气,存在操作环境要求并具安全隐患,通常使用具有稳定电位的电极作为常用的参比电极。
饱和甘汞电极(SCE)和 Ag | AgCl 电极,就是最有代表性的常用参比电极。银氯化银电极的电极电位的关系式,已经在前面的电极分类中的金属及其难溶盐构成的电极部分介绍过了。
甘汞电极也是属于这一类电极。是由金属汞和氯化亚汞难溶盐浸入在饱和氯化钾溶液中构成,SEC电极构成可以表示为 : Pt (or Cu)导线| Hg | Hg2Cl2(s) | KClsatd ||
由于金属汞为液态,需要与铂金线或铜线连接后,才能与外电路连接使用,所以可在左侧加上Pt (or Cu)导线的记号。
电极反应式在式17中表示. 电极电位的Nernst方程式用式18表示。
饱和甘汞电极(SCE)和 Ag | AgCl 电极,就是最有代表性的常用参比电极。银氯化银电极的电极电位的关系式,已经在前面的电极分类中的金属及其难溶盐构成的电极部分介绍过了。
甘汞电极也是属于这一类电极。是由金属汞和氯化亚汞难溶盐浸入在饱和氯化钾溶液中构成,SEC电极构成可以表示为 : Pt (or Cu)导线| Hg | Hg2Cl2(s) | KClsatd ||
由于金属汞为液态,需要与铂金线或铜线连接后,才能与外电路连接使用,所以可在左侧加上Pt (or Cu)导线的记号。
电极反应式在式17中表示. 电极电位的Nernst方程式用式18表示。
由于标准氢气电极是电位比较的最初标准,而各种常用参比电极的电位存在差异,将使用常用参比电极测得的相对电位,换算成对标准氢电极的电位后,更加方便所得电位间进行比较。
图7为 将常用参比电极测得的电位转换成vs. SHE 电位的方法 示意图。
例如,使用银氯化银电极测得的电位为0.5V, 换算方法为,将该测得值加上该银氯化银电极对标准氢电极的电位值,例如图6中的+0.228V,得到0.728V vs.SHE
图7为 将常用参比电极测得的电位转换成vs. SHE 电位的方法 示意图。
例如,使用银氯化银电极测得的电位为0.5V, 换算方法为,将该测得值加上该银氯化银电极对标准氢电极的电位值,例如图6中的+0.228V,得到0.728V vs.SHE
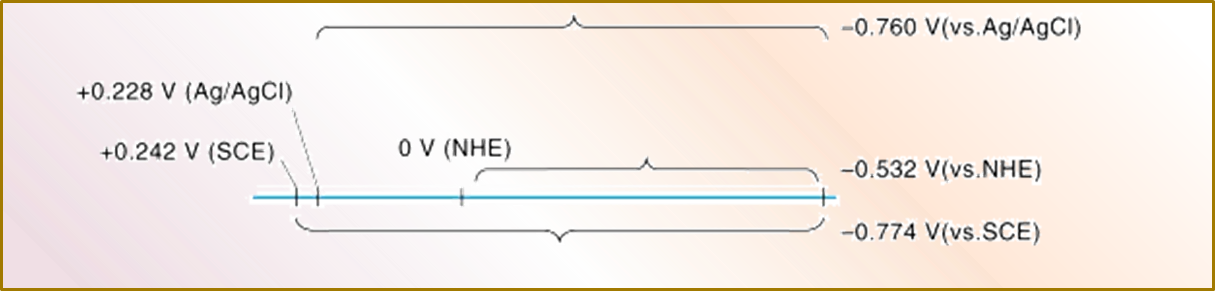
图7 将常用参比电极测得的电位转换成vs. SHE 电位的方法
(2) 电位测量

图8 电位测量装置
图8 为电位测量装置的示意图。左侧电极为参比电极,右侧电极为指示电极即电极电位会随着待测化学物种的浓度而变化的电极。
◇ 参比电极体系:电位稳定,操作方便,可代替SHE使用的电极,比如Ag | AgCl电极等。
◇指示电极体系:电极电位会随着待测化学物种的浓度而变化的电极。
[例如] 氧化还原电极(铂电极等)→ 电极电位会因溶液中氧化/还原物种的浓度比变化而改变。(Pt | Ce4+, Ce3+)
由于图8的电位测量池包含了液接电位 (Ej)。那么电池的电动势可以用式19表示(其中包含了盐桥的液接电位 Ej)。
◇ 参比电极体系:电位稳定,操作方便,可代替SHE使用的电极,比如Ag | AgCl电极等。
◇指示电极体系:电极电位会随着待测化学物种的浓度而变化的电极。
[例如] 氧化还原电极(铂电极等)→ 电极电位会因溶液中氧化/还原物种的浓度比变化而改变。(Pt | Ce4+, Ce3+)
由于图8的电位测量池包含了液接电位 (Ej)。那么电池的电动势可以用式19表示(其中包含了盐桥的液接电位 Ej)。
如果 Ej 是恒定的,无论被测样品如何(即加入了足够的支持性电解质),那么Ej可以看作是一个常数。
可以将常数项(Eref, Ej, Eoind)统合为k,因为可以用电极直接测量的不是浓度而是活度,那么电池的电动势可以用式20表示。
(20)
