电位控制介绍连载
篇将首先介绍 电极电位的二电极,三电极控制方法,并简述了双电层的特点。然后介绍物质传输的各种方式,以及反映物质传输对电极反应影响的守恒定律和菲克定律。
最后对在处理电极反应时应将传质过程和界面电子转移反应过程进行综合考虑进行简要的说明。
- 第一篇 电极电位的控制法(1):二電極方式
- 第二篇 电极电位的控制法(2) 双电层&三电极方式
第一篇 电极电位的控制法(1):二電極方式
此外,还要考虑到电极界面处的静电场问题,还会涉及到电磁学知识等等...
“电化学反应”一个是以各个领域的学术研究为背景的边界交叉学术领域。
由于上述原因使得人们感到电化学难以入门。 特别是得知需要掌握各种知识后可能会变得更加无所适从。 在本系列中,我们采用了循序渐近的方法进行说明,希望能帮助大家学到所需要的知识。
本篇将在前半部分讨论电位控制和传质过程,在后半部分进行传质过程的讨论,并且阐述它是如何与反应动力学联系起来的。 为在后续的各种测量法的学习打下基础。
在上一篇中以电流和过电位为重点介绍了电化学反应的动力学。 如果说电化学测量方法的基础是寻找“电位”和“电流”之间的相关性,那么正确“测量”或“控制”电极电位是绝对必要的。 让我们考虑如何实现这一点。
首先,让我们回顾一下电极电位的定义(图1)。 电极电位 E是一个定义 为电极(导体)相的内部电位 φM 与溶液相的内部电位 φS之差的量(式1)。
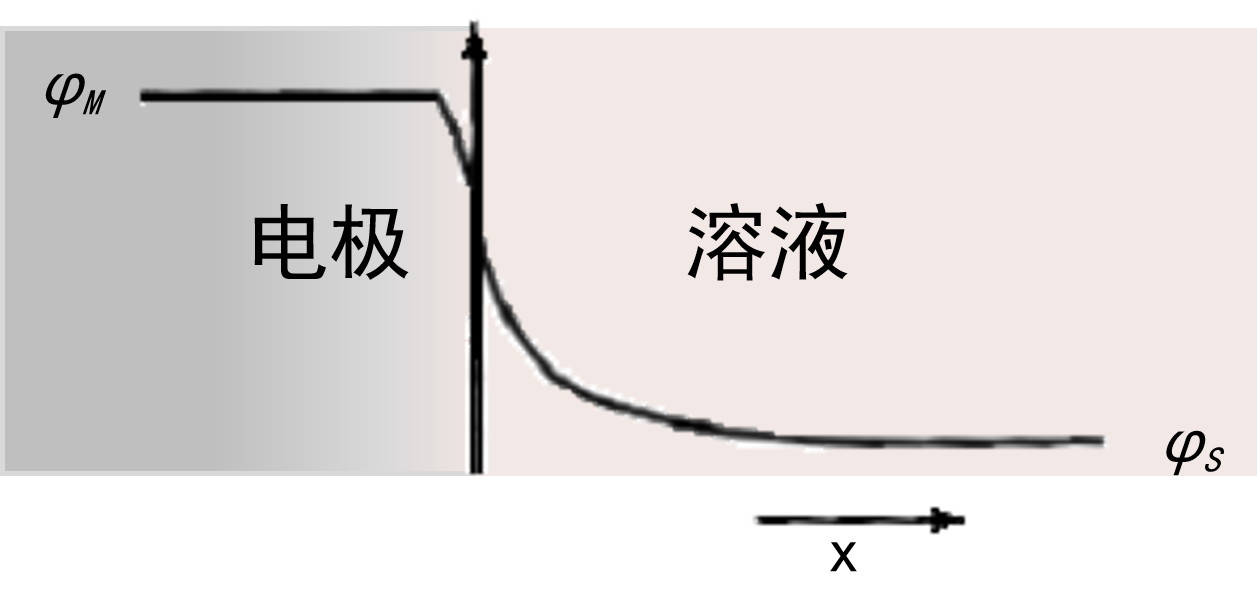
图1 金属电极界面层电势随距离的变化(Jellium模型)
这仅仅是一个定义,因为我们无法直接测量两个不同相位之间的电位差。 然而,由于电极反应的热力学和动力学是基于电极电位来讨论的,因此在实验中需要以某种方式调节与此相对应的量。
顺便提一下,我们之前在学校学习的电池和电解反应中,总是由一个将两个电极浸入电解液中的体系构成。 这是因为它不能仅用一个电极来进行测量或控制。 比如,在电极的两个端子之间连接电压表并测量电位差时,将其中一个电极用作参考标准(即零)。测量与另一个的相对电位差。 在电解过程中,外部电源的接地端子连接到其中一个电极端子,并在另一个连接端子上加上一个电位差。 换句话说,总有一个电极充当“电位参考”。 如果此参比电极的内部电位为φM2,则电极电位为式2,同样另一个电极的电位可以定义为式3.
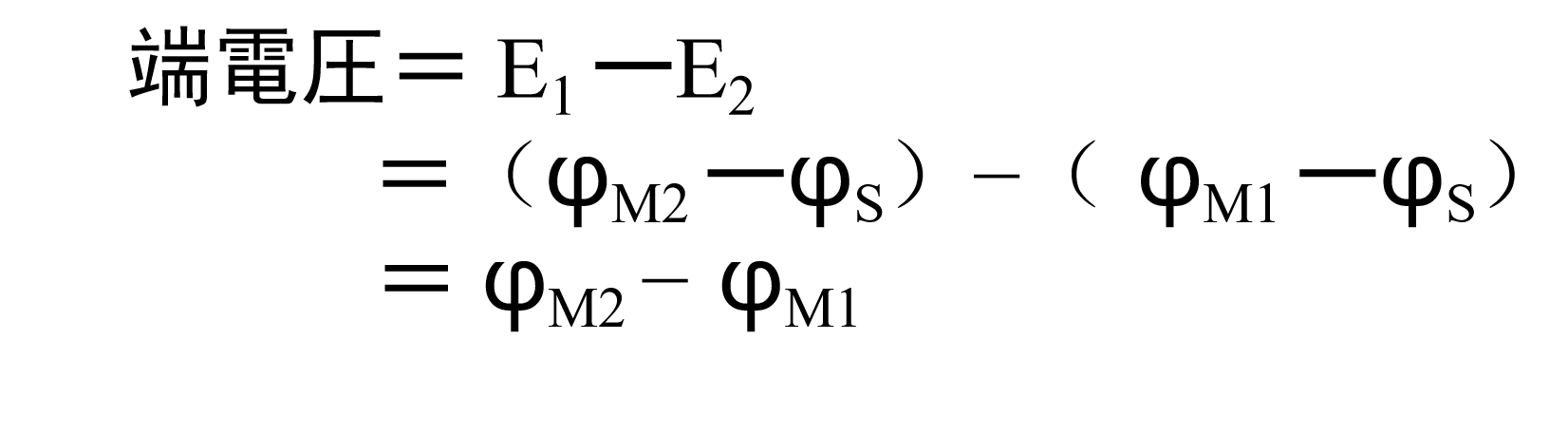
(4)
取两者之差,得到式4,溶液的内电位φS从方程中消失,测得的端电压(或加在两端的电压)稳定在两极间的内电位之差.
也就是说,在实际实验中,我们不需要知道φ S 的值。
然而,我们不能忘记由公式 (2) 和 (3) 定义的各个“电极电位”。
电压表测得的端电压似乎确实反映了两个电极之间的内部电位差,但在电池内部却是各个电极电位之和(公式中的差值)。 两个电极的贡献不能进行单独表征(图 2)。
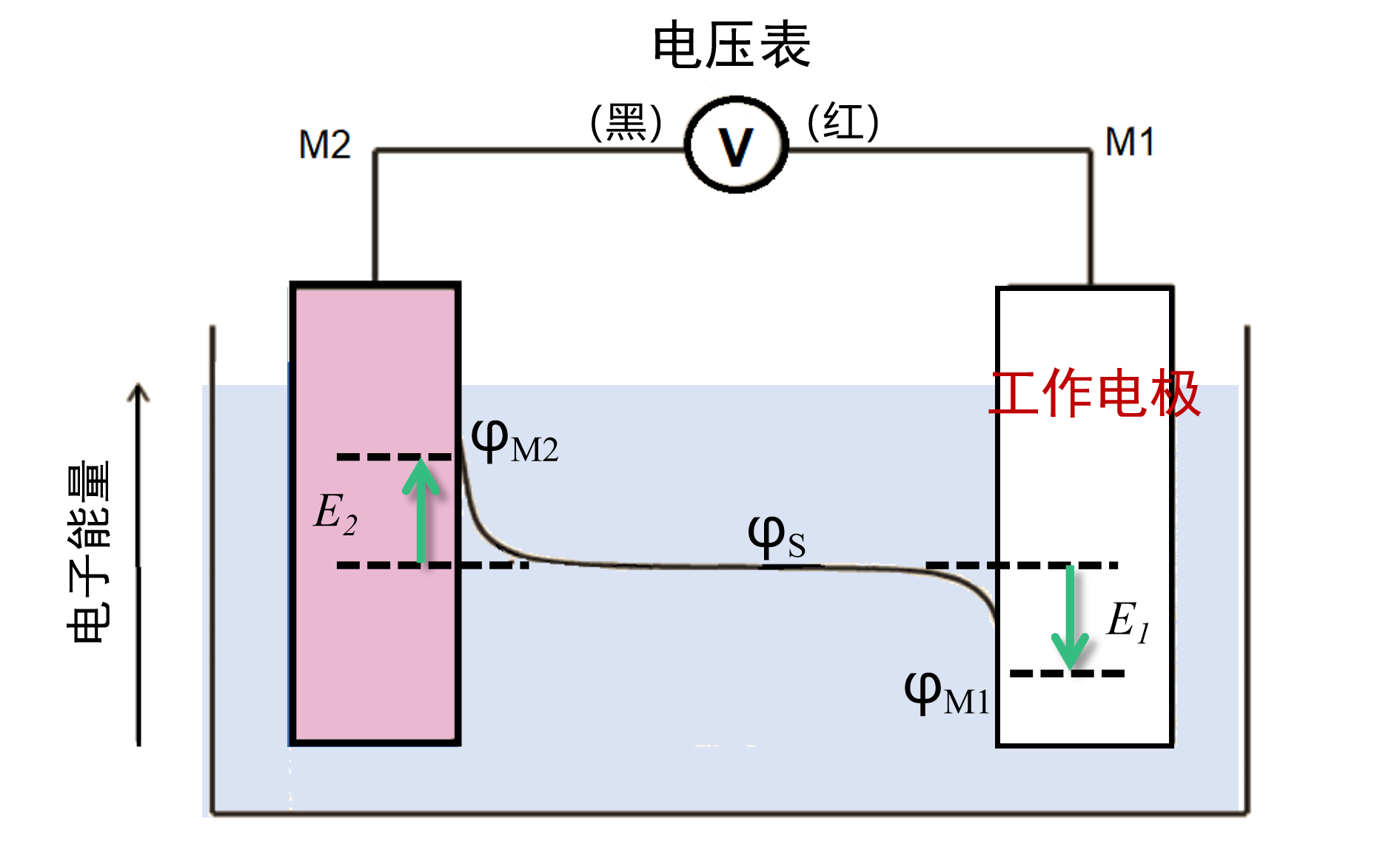
图2. 端电压的测量示意图。
用电压表测量右侧的 M1 相对于左侧的 M2的电位。
溶液内部的电位分布示意图,对应与假设 M1 相对于 M2 具有正电位时的情况。
导致电极电位波动的主要因素是法拉第电流的流动。 正如我们上次看到的,过电压总是在电流流动时发生。 各电极发生的氧化还原反应的种类一般不同,过电压的大小也各不相同。 从外部施加的电位差将适当地分布到这两个电极上(图 3)。
该比率也将根据电流和时间的量而变化。 在这种情况下,不可能只关注工作电极。
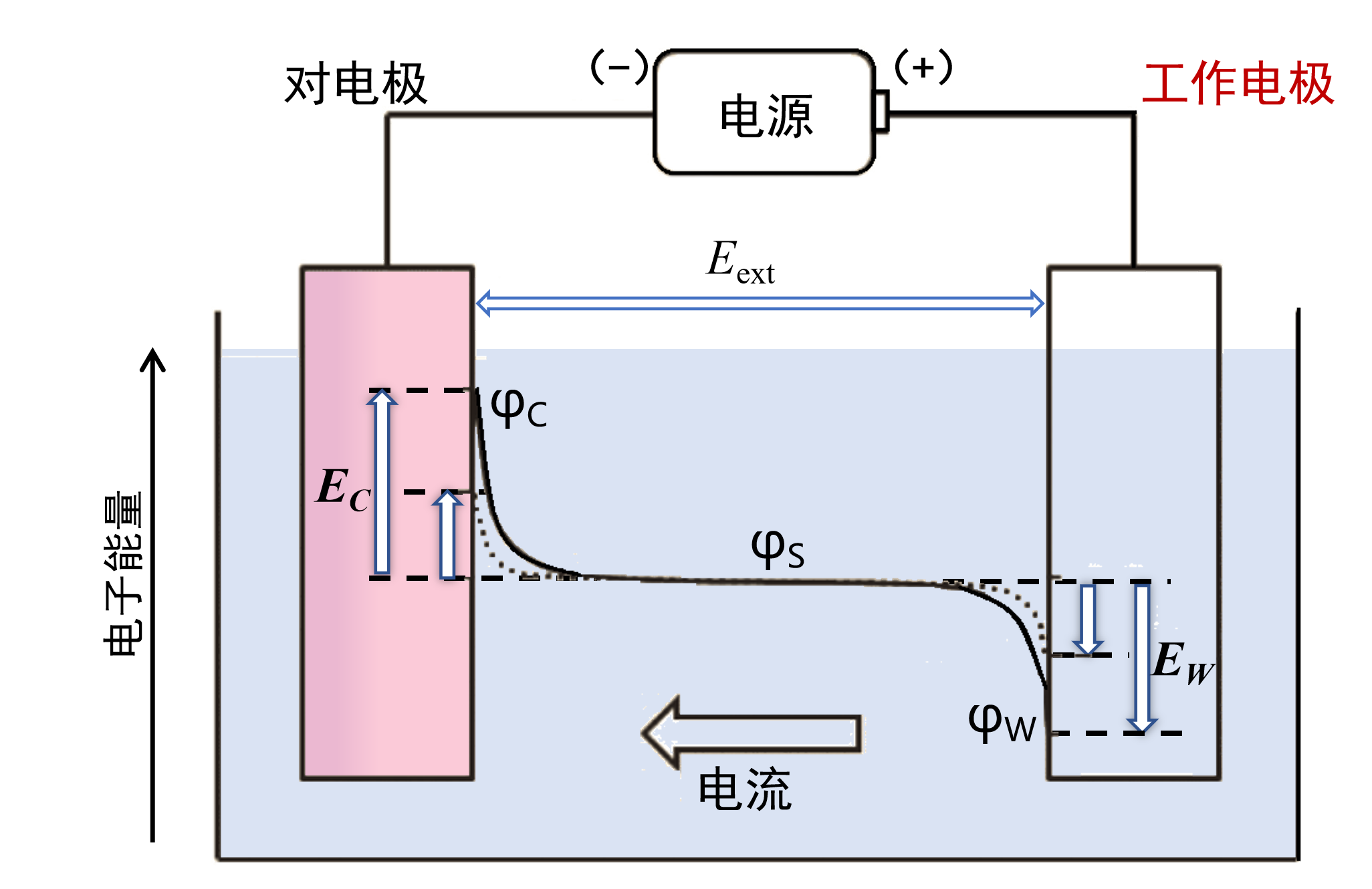
图3.外加电压在二电极法中的应用。
当反应电流流动时,每个极产生过电压,因此 EW 和 EC都会发生变化。(|ΔEext| = |ΔE EW| + |ΔEC|).
现在,让我们回忆一下以前说过的极化。 极性大的电极需要外加大的过电压才能产生小电流,而极性小的电极只需要外加小的过电位就能产生大电流。 换句话说,即使有电流流动,电位也只会轻微波动。 因此,如果使用极性较小的电极作为对电极进行测量,会发生什么情况? 如图 4所示,外加电压差 ΔEext 将更多地用于工作电极的过电压变化,而不是对电极。
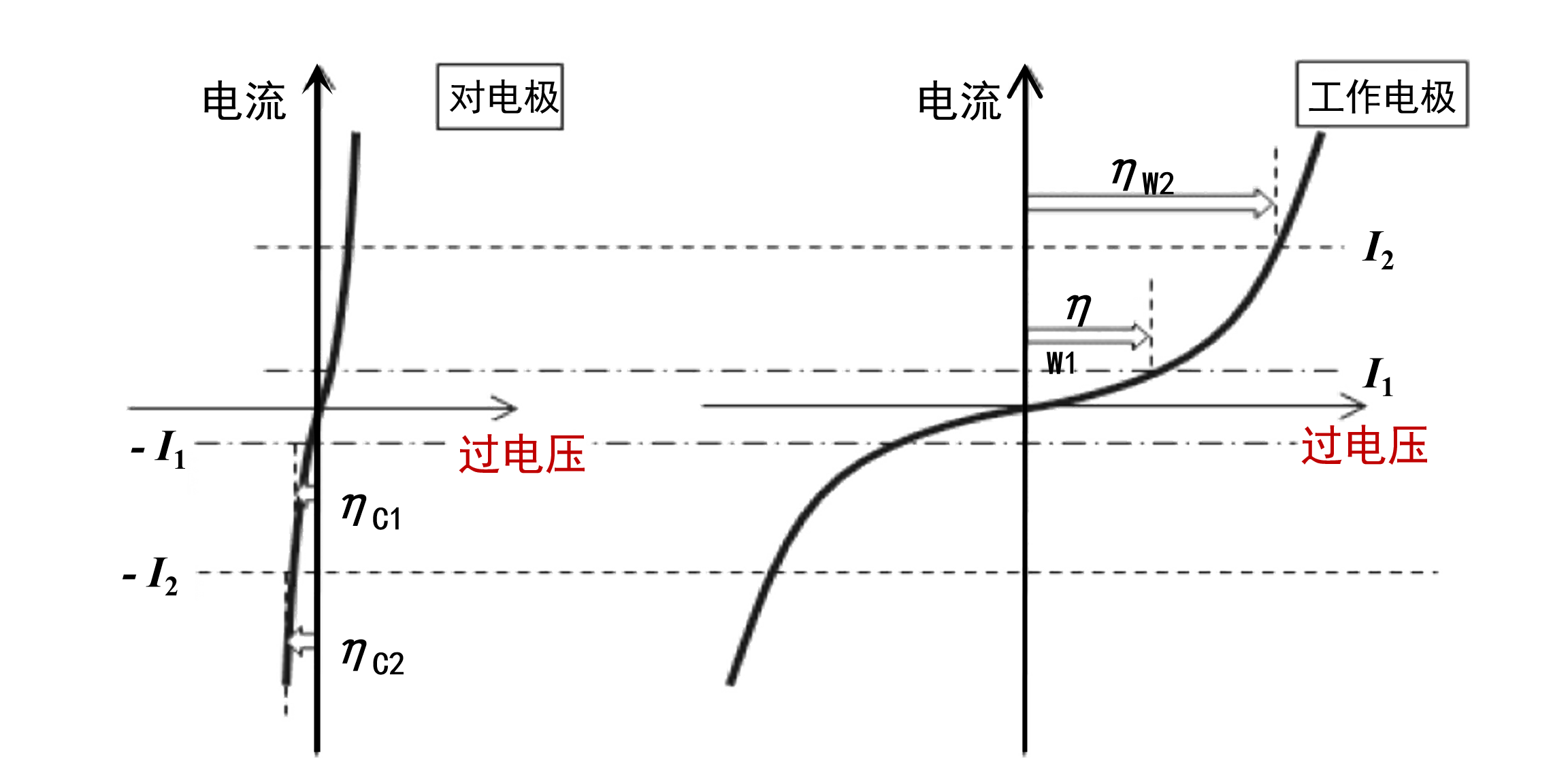
图4 不同极性电极的组合。
例如,当氧化电流 I 在工作电极上流动时,还原电流 -I 在对电极上流动。 如果对电极的极性足够小于工作电极的极性,则通过任意大小的电流|I|所需的活化过电压为|ηC|<<|ηW|,因此可以认为是|ΔE|∝|ηW|。
第二篇 电极电位的控制法(2):双电层&三电极方式
◆双电层
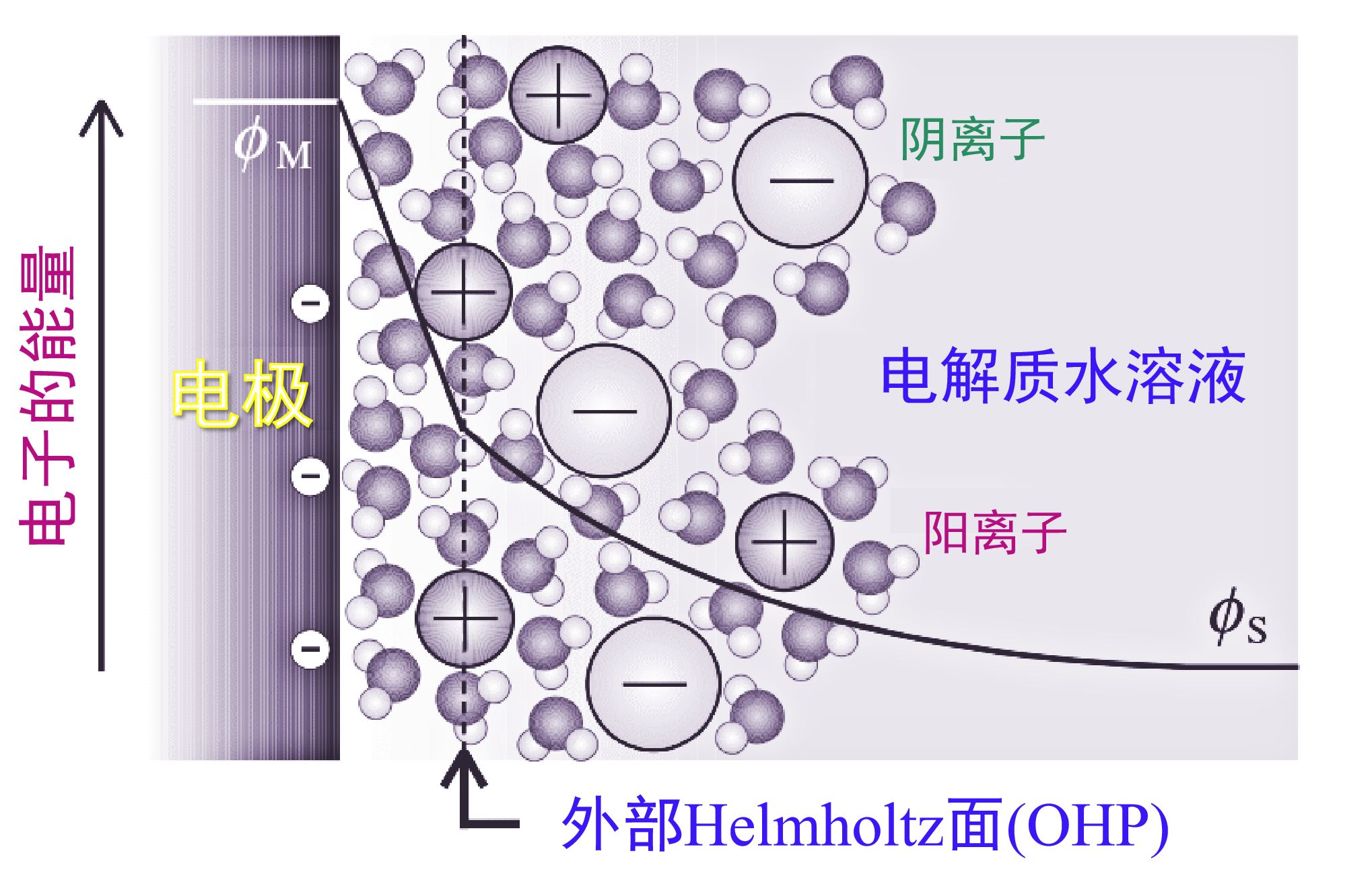
图5 双电层示意图。
水合阳离子与电极紧密接触的表面称为外亥姆霍兹表面。
在许多电子转移反应中,当物质接近这个距离时会与电极进行电子交换。
将带电的金属电极插入电解液时,周围的阴离子和阳离子会受到静电场的影响。由于离子在热运动的同时被吸引或推向金属表面,以抵消金属表面的过量电荷,使离子在最稳定的状态下达到平衡分布。 补充说明一下,即使没有特意让金属带电,金属相和溶液相的内部电位通常是不同的,因此只需将金属插入溶液中就会发生相同的现象。
通常,发生这种重新分布的范围是距电极表面几纳米的范围,这抵消了表面上的大部分多余电荷。结果,电位分布在电极界面处显示出非常陡峭的距离依赖性。只要离开稍稍电极一点距离,就接近溶液体的内部电位。(图4)。产生这种电位梯度的狭窄的界面区域称为双电层。由于反应物O 和 R 与电极进行电子交换的地方处于 如此大的电位梯度之中,因此电极电位的变化就能够有效地改变电子转移反应的活化能。
◆三电极方式
在前面看到的二电极方式中,施加到对电极的过电压的波动是一个测量中的问题。 但是,只要有电流流动,反应就会继续发生。,是否有什么好的方法可以在 即使有电流通过工作电极的情况下,仍可以保证工作电极的电位不变呢?
如果吧对电极所起的“电位参考”和“电流处理”这两个作用分成两个电极的话,会如何呢?换句话说,让我们提供一个用于调节工作电极电位的参考电极(也称为标准电极)和一个对电极(或称辅助电极),作为流过工作电极的电流的逃逸通道。并且,通过设计使电流尽可能不流向参比电极,则电极电位将始终保持稳定。另一方面,即使电流流过辅助电极并且电位随之波动,也无需担心(图6)。
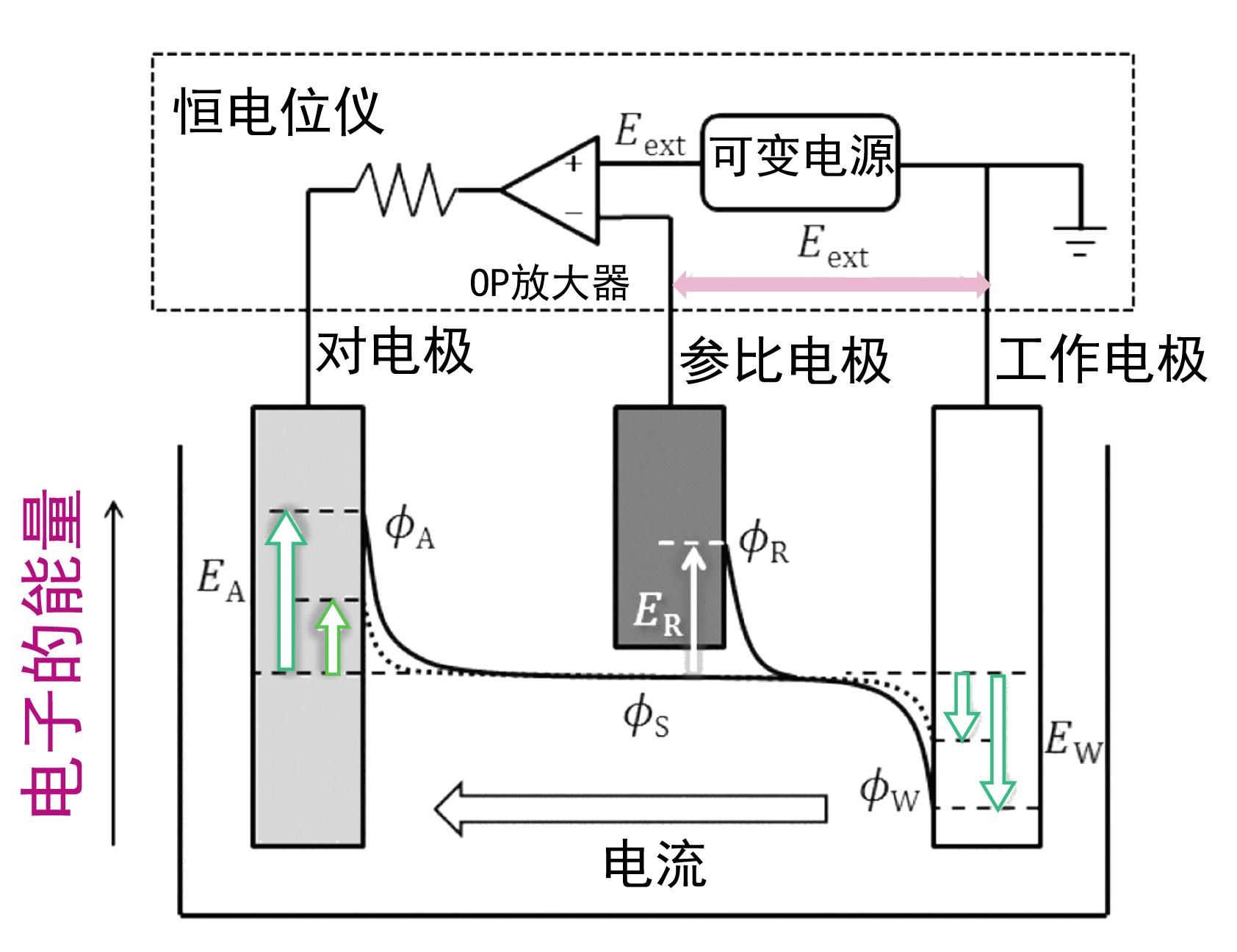
图6. 三电极法的电位控制和传质过程
由于OP放大器的作用,可变电源产生的电压Eext总是出现在工作电极和参比电极之间(EWーER=Eext)。
另一方面,由于没有电流通过参比电极,ER 是不变的。 因此,|ΔEext|≈|ΔEW|。
此外,即使电流在工作电极和辅助电极之间流动并且EA波动,工作电极的电位也不受影响。
为了实现这样的控制系统,需要设计外部电路,市售的恒电位仪具有该功能。目前的电化学测量通常通过使用恒电位仪的三电极法进行。恒电位仪可以自己制作,如果自己尝试做电路,可以很好的理解其工作原理,对于判断平时测量得到的数据的好坏很有用。
对电位控制讨论到此结束.
