7. 液接电势和试样架桥管
Laboratory Of Research & Development, BAS Inc.
Professor Noriyuki Watanabe
Professor Noriyuki Watanabe
使用一个参比电极必然会在参比电极和测试溶液之间的存在液-液界面。当参比电极使用盐桥的时,增加了额外的界面。在这样的界面上不可避免地产生液接电势,液接电势的大小取决于电解质溶液的组成。不同组分的离子通过界面时,各自的离子迁移率的不同是产生液接电势的根源。根据亨德森方程,使用离子迁移率和组成电解质的浓度,计算出液接电势的大小。虽然方程看起来复杂,包括离子迁移率,离子电荷和组成离子的浓度,它是被简化的,因为只有几个主要组成部分是有效的。
当你在参比电极和测试溶液间使用盐桥时,为了尽量减低液接电势而明智的选择电解质成分很重要。往往选择K+、NH4+、Cl-、 NO3-的组合,是因为他们具有类似的迁移率。
由于KCl的溶解度非常低(水中的饱和浓度大约为4.8 M),考虑到成本费用有时会使用CsCl或RbCl。Rb+ 和 Cs+的迁移率几乎和Cl-相同。当KCl = 1.000时的其他离子的相对迁移率如表所示。
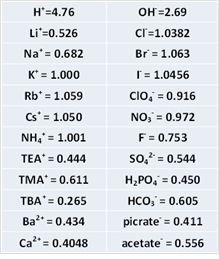
当试验溶液中有高氯酸阴离子时用NaCl来替代KCl。其原因是高氯酸钾的溶解度相当低,而高氯酸钠的溶解度约为一百倍。由于KClO4的溶解度低,通过这个对策来降低接液部析出的风险。使用哪一个需要权衡利弊。
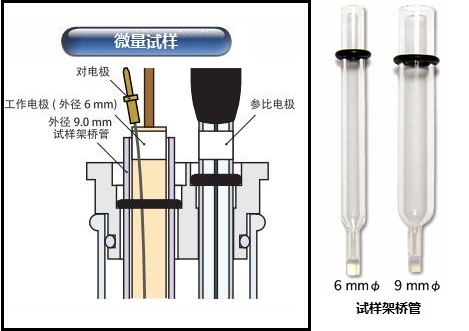
试样架桥管本身可通过自行配制内溶液(选择溶剂、支持电解质、银盐)作为银离子参比电极使用,9mm外径的试样架桥管可用于插入6 mm外径的参比电极,起到盐桥的作用。
此外,使用外径分别为 9 mm和6 mm的试样架桥管可实现微量样品的的电化学测量。 例如,使用SVC-2伏安电化学池,在9 mm试样架桥管中放置外径为6mm的工作电极和对电极,将参比电极放入SVC-2伏安电化学池构成双室池,可进行100~200 微升试样溶液的电化学测量。