第十二篇 溶剂对电极反应的的影响效果
溶剂性质,支持电解质性质,以及两者的行为变化对电极反应会产生各种各样的影响。
先来看溶剂对电极反应的的影响效果
●对金属离子和配合物的电极反应的影响
1) 对于金属离子还原成金属((或金属汞齐)的电位,会随着金属离子在溶剂中的溶剂化作用的增强而向负电位方向移动,这种电位的负移与离子的溶剂化能之间存在着热力学的对应关系。 溶剂对极谱半波电位的影响经常被用为比较金属离子溶解能化的手段。
2)由于在非质子溶剂中不易发生因溶剂产生的分解,那些在水溶液中因发生水解而得不到良好极谱图的碱土金属、铝、锆等离子,也能得到较好的还原波。
还有,那些会与水反应的活性金属,比如碱金属Na,K等,也可以在非质子溶剂中在电极上析出。
3) 在非质子性溶剂中,通过电极反应产生的低价态金属配合物可以稳定存在[13][14] 。
例如二价铁的联吡啶配离子[Fe(bipy)3]2+在水溶液中发生2电子还原,一步生成零价铁的配合物,然而在非质子性溶剂中则会发生1电子3步的可逆还原步骤,产生比较稳定的[Fe(bipy)3]- 如下。
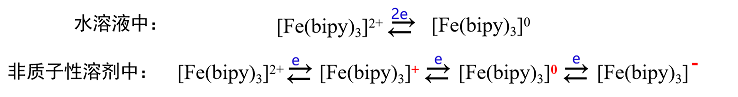
此外Cr、Ni、Ru 联吡啶络合物等各种络合物也同样如此。
这是因为非质子溶剂的酸性较弱,难以与配合物的配体(碱)反应。从可以得到不依赖于溶剂的电位参考标准的角度来看,这些反应体系值得引起大家的注意。
此外,由于那些不溶于水的配合物和有机金属化合物通常可以溶解在有机溶剂中,因此对这些电极反应进行详细的研究。
●对有机化合物的电极反应影响
许多有机化合物(R)在水溶液中通过2电子还原,一步生成加氢还原产物 RH2 (方程式 11)。
然而在非质子性溶剂中,还原反应的机理,则会分成2个一电子还原步骤,先是1电子还原生成一个相当稳定的阴离子自由基,再进一步得到一个电子还原成R2-阴离子。
这一现象在有机溶剂应用于电极反应的历史上非常重要,并被广泛地研究。通过研究发现,随着溶剂受体数的增加,第一步还原生成阴离子自由基的半波电位会 出现正向线性移动。 Aoyagi 等,用铂电极在 0.4M 四丁基高氯酸铵盐的DME溶液中,实现了环十轮烯烃分子的4个1电子可逆氧化还原步骤。并在 DME 中得到了相对稳定的相当于R4-的活性阴离子。
还有, 在极性疏质子的非质子性,例如:乙腈(AN) 碳酸丙烯脂(PC) 硝基甲烷 (NM),环丁砜 (TMS) 等溶剂中,通过使用适当的支持性电解质,可以测量至相当高的正电位,甚至能观察到难以氧化的苯的氧化。
亲质子性溶剂和水溶液中: R•+ + 溶剂 ⇔ R•+溶剂
疏质子性溶剂中的自由基聚合: nR•+ → Rn
(15)
(16)
有机化合物的氧化常常会在第一步生成阳离子自由基(R⇄ R+ + e),其通常比相应的阴离子自由基更不稳定。 在亲质子性溶剂和水溶液中,这些阳离子自由基会与溶剂发生反应。但是如果在疏质子性溶剂中,因为溶剂和阳离子自由基之间不会发生反应,此时可以发生自由基的聚合反应。
因此,进行氧化反应测量时,有必要使用给体性(碱性)强弱合适的溶剂,以实现目标的反应[15]。
参考文献
[13] T.Saji and S. Aoyagui,Inorg.Nucl. Chem. Lett. 2, 359 (1966).
[14] T.Saji and S. Aoyagui,Electrochim. Acta 13, 335(1968).
[15] T.Saji and S. Aoyagui,J. Electroanal. Chem.102, 139(1979).
